 更新時間:2025-09-19
更新時間:2025-09-19 點擊次數:105
點擊次數:105
高遷移率族蛋白B1(High Mobility Group box 1 protein,HMGB1)是一種高度保守的核蛋白,存在于所有細胞類型中,其因在凝膠電泳過程中的快速遷移而得名[1]。
HMGB1作為含量豐富的HMG蛋白家族成員,在典型哺乳動物細胞中的豐度可達約1×10?個細胞,其分布密度約為每10-15個核小體對應1個HMGB1分子[2]。HMGB1廣泛表達于各種器官中,通常存在于細胞核中[3]。HMGB1蛋白是由一條215個氨基酸組成的單鏈多肽,其結構包含三個特征性功能域:N端A-box(AA1-79)、中央B-box(AA89-162)和C端酸性尾(AA186-215)[4]。人類HMGB1基因定位于13q12染色體,其基因組包含5個外顯子和4個內含子。此外,HMGB1基因啟動子區域不僅具有典型的TATA盒啟動子,其還整合了數個轉錄因子結合位點以及一個沉默元件,這種復合調控機制使得HMGB1于穩態條件中可維持相對平穩的基礎表達量[5]。與此同時,HMGB1還在不同物種中展現出高度的序列同源性,其中,大鼠與小鼠的HMGB1蛋白序列一致,同源性高達100%,且相較于人類HMGB1蛋白,僅存在C末端重復序列2個殘基的置換差異[6]。
功能及作用機制
Ⅰ、功能
HMGB1于亞細胞定位中呈現功能多樣性:在細胞核中主要參與DNA損傷修復、穩定染色質的結構等過程;在細胞質中則發揮免疫調節,線粒體穩態維持、神經細胞生長促進等生理功能[7]。此外,當HMGB1通過壞死、凋亡細胞釋放或免疫細胞主動分泌至胞外后,其可與晚期糖基化終產物受體(Receptor for Advanced Glycation End Products,RAGE)特異性結合,啟動下游信號通路。作為多效性細胞信號轉導樞紐,RAGE-HMGB1信號通路可在炎癥應答、細胞分化調控及腫瘤轉移等病理過程中發揮關鍵作用。最近的研究表明,中性粒細胞及巨噬細胞中HMGB1可通過Toll樣受體(TLR)-2和TLR-4受體復合物激活MyD88依賴性的信號級聯反應,從而進一步驅動NF-κB轉錄因子的活化[8]。
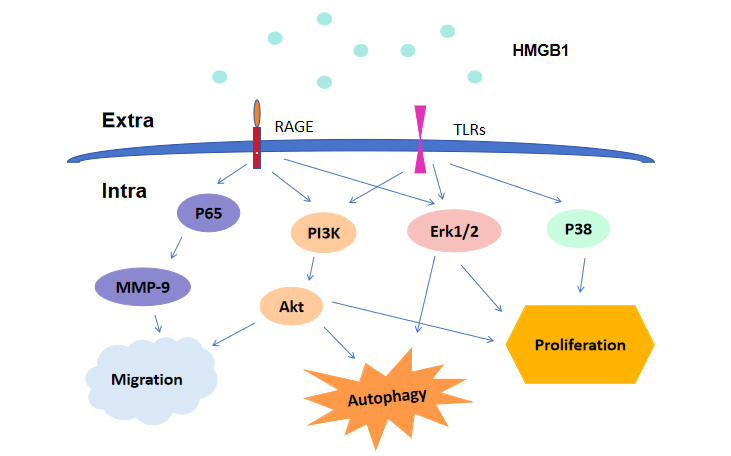
圖1.HMGB1調節細胞增殖、細胞死亡和轉移[9]
Ⅱ、作用機制
HMGB1的生物學功能主要由PI3K/Akt、NF-κB(p65)和MAPK(ERK1/2,p38)信號轉導通路介導。
① PI3K/Akt信號通路
HMGB1通過結合RAGE或TLR2/4受體,直接或間接激活PI3K/Akt通路,影響細胞存活、炎癥和疾病進展。PI3K由一個催化結構域(p110)和一個調節結構域(p85)組成,可被G蛋白偶聯受體、RTK、IGF-R和B細胞受體激活。激活的PI3K催化PIP2向PIP3的轉化,生成的PIP3進一步激活PDK1,從而介導PDK1對AKT蛋白Thr308位點的磷酸化激活。此外,PDK2也可通過磷酸化AKT蛋白的Ser473位點,激活PI3K/AKT信號通路。激活的AKT可通過與許多下游信號分子(如p21、p27、TGFβ、ataxin-1、GABA受體、Bad、NF-κB和mTOR)相互作用來調節增殖、凋亡、遷移、侵襲、分化與血管生成等細胞生物學功能。
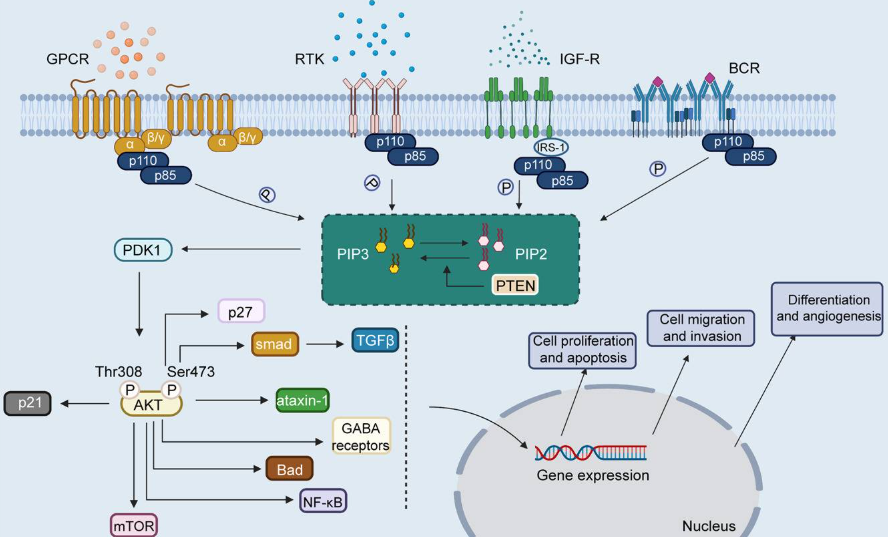
圖2.PI3K/AKT信號通路的激活過程[10]
②經典NF-κB信號通路
HMGB1在炎癥微環境中通過激活NF-κB信號網絡發揮關鍵調控作用。在經典NF-κB激活通路中,IκB激酶(IKK)復合物作為核心催化單元,其結構包含兩個催化亞基(IKKα/IKKβ)和一個調控亞基(IKKγ)。當IKK復合體被激活后,通過特異性磷酸化IκB蛋白的N端調控域,觸發IκB的泛素化修飾及蛋白酶體依賴性降解。這一級聯反應最終導致p50/RelA異源二聚體從IκB介導的胞質滯留中釋放,釋放后的NF-κB二聚體可通過特定的翻譯后修飾作用,進一步促進其易位到細胞核。進入細胞核后,NF-κB二聚體能夠與靶基因啟動子或增強子區域的特定κB位點結合,從而驅動靶基因的轉錄。
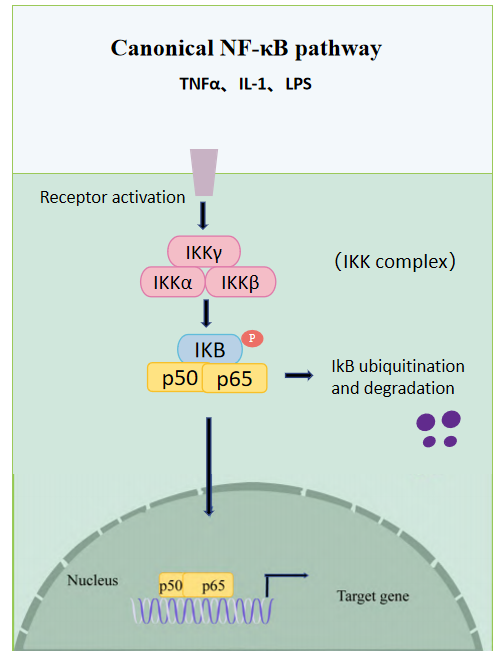
圖3.經典NF-κB信號通路機制示意圖[11]
③MAPK信號通路
MAPK的激活是細胞內磷酸化級聯反應的最終步驟,經典的MAPK級聯反應包括MAPKKKK(如Ras、Rho)一MAPKK激酶(MAPKKK)一將MAPKK絲氨酸/蘇氨酸磷酸化一激活的MAPKK將MAPK的蘇氨酸/酪氨酸雙重磷酸化,激活MAPK。MAPK信號轉導通路中存在的增強因子,可與MAPKKKs、MAPKKs和MAPKs結合,增加上游激酶對它們的激活能力。
MAPK(絲裂原活化蛋白激酶)通路有三級的信號傳遞過程:MAPK,MAPK激酶(MEK或MKK)以及MAPK激酶的激酶(MEKK或MKKK)。這三種激酶能依次激活,共同調節著細胞的生長、分化、應激、炎癥反應等多種重要的生理/病理效應。
到目前為止,研究廣泛的哺乳動物MAPK組是ERK1/2、JNK和p38亞型,其中HMGB1執行ERK1/2,p38通路。

圖4.有絲分裂原、細胞因子和細胞應激促進不同MAPK通路的激活[12]
臨床應用
01
炎癥性疾病
HMGB1在多種炎癥性疾病中發揮核心作用。它通過激活免疫細胞、促進炎癥因子釋放和加劇組織損傷,參與膿毒癥、類風濕性關節炎(RA)和炎癥性腸病(IBD)等疾病的發病過程。因此HMGB1在炎癥性疾病中既是關鍵促炎介質,也是潛在治療靶點。
02
自身免疫性疾病
HMGB1通過促進自身抗原呈遞、增強炎癥反應和破壞免疫耐受,加劇疾病進展,并在系統性紅斑狼瘡、糖尿病發揮重要作用。HMGB1促進腎臟巨噬細胞浸潤和系膜細胞增殖,加劇腎損傷,同時HMGB1在1型糖尿病患者血清和胰島中高表達,促進胰島β細胞破壞,并在肥胖和2型糖尿病患者血清中升高。這說明HMGB1在自身免疫性疾病進展中起關鍵作用。
03
敗血癥和失血性休克
HMGB1在敗血癥和失血性休克表現出特征性的延遲釋放模式,在TNF刺激巨噬細胞下介導晚期炎癥反應。此外,HMGB1不僅自身作為晚期炎癥介質,還能刺激其他致炎因子釋放,形成正反饋循環,在膿毒癥繼發性器官損傷和休克后炎癥反應中起關鍵作用。
04
腫瘤的雙重作用
HMGB1在腫瘤微環境(TME)中具有雙重作用:一方面HMGB1可通過促進腫瘤細胞增殖、誘導新生腫瘤血管生成、塑造免疫抑制環境以及增強促侵襲轉移特性等機制發揮促癌作用;另一方面,HMGB1可介導免疫原性細胞死亡(Immunogenic Cell Death,ICD),提高抗腫瘤免疫力,起到抗癌的作用。這些功能可為靶向干預治療腫瘤提供重要理論依據。
05
神經元發育調控功能
HMGB1在神經系統中呈現特異性的亞細胞分布特征,其高表達于神經元胞體與軸突的胞質區室,并與外周膠質細胞器存在共定位現象。功能研究表明,在大鼠原代神經元體外培養體系中,抗HMGB1抗體可顯著抑制軸突生長。這說明HMGB1在神經生長發育過程中起著非常重要的作用。
06
影響凝血、纖溶系統功能
HMGB1是一種強有力的肝素結合蛋白,不僅可誘導內皮細胞釋放纖溶蛋白酶原激活因子抑制物和組織型纖溶蛋白酶原激活物,還能間接促進細胞表面纖溶酶原的產生。HMGB1通過結合肝素并調控內皮細胞釋放PAI-1和t-PA,同時促進纖溶酶原生成,破壞凝血-纖溶平衡,增加血栓形成風險。這表明HMGB1在凝血、纖溶系統進展中起關鍵作用。
相關產品
貨號 | 中文名稱 | 英文名稱 |
SEKM-0145 | 小鼠高遷移率族蛋白 B1檢測試劑盒 | ElaBoX? Mouse HMGB1 ELISA Kit |
SEKH-0409 | 人高遷徙率族蛋白 B1檢測試劑盒 | ElaBoX? Human HMGB1 ELISA Kit |
SEKR-0074 | 大鼠高遷移率族蛋白 B1檢測試劑盒 | ElaBoX? Rat HMGB1 ELISA Kit |
參考文獻
[1]Yang H, Wang H, Andersson U. Targeting Inflammation Driven by HMGB1. Front Immunol. 2020 Mar 20;11:484.
[2]Thomas JO, Travers AA. HMG1 and 2, and related 'architectural' DNA-binding proteins. Trends Biochem Sci. 2001 Mar;26(3):167-74.
[3]Lotze MT, Tracey KJ. High-mobility group box 1 protein (HMGB1): nuclear weapon in the immune arsenal. Nat Rev Immunol. 2005 Apr;5(4):331-42.
[4]Kang R, Chen R, Zhang Q, Hou W, Wu S, Cao L, Huang J, Yu Y, Fan XG, Yan Z, Sun X, Wang H, Wang Q, Tsung A, Billiar TR, Zeh HJ 3rd, Lotze MT, Tang D. HMGB1 in health and disease. Mol Aspects Med. 2014 Dec;40:1-116.
[5]Ferrari S, Finelli P, Rocchi M, Bianchi ME. The active gene that encodes human high mobility group 1 protein (HMG1) contains introns and maps to chromosome 13. Genomics. 1996 Jul 15;35(2):367-71.
[6]Bianchi ME, Falciola L, Ferrari S, Lilley DM. The DNA binding site of HMG1 protein is composed of two similar segments (HMG boxes), both of which have counterparts in other eukaryotic regulatory proteins. EMBO J. 1992 Mar;11(3):1055-63.
[7]TANG D, KANG R, ZEH H J, et al. The multifunctional protein HMGB1: 50 years of discovery [J]. Nat Rev Immunol, 2023, 23(12): 824-41.
[8]SIMS G P, ROWE D C, RIETDIJK S T, et al. HMGB1 and RAGE in inflammation and cancer [J]. Annu Rev Immunol, 2010, 28: 367-88.
[9]Wu L, Yang L. The function and mechanism of HMGB1 in lung cancer and its potential therapeutic implications. Oncol Lett. 2018 May;15(5):6799-6805.
[10]Xue C, Li G, Lu J, Li L. Crosstalk between circRNAs and the PI3K/AKT signaling pathway in cancer progression. Signal Transduct Target Ther. 2021 Nov 24;6(1):400.
[11]YU H, LIN L, ZHANG Z, et al. Targeting NF-κB pathway for the therapy of diseases: mechanism and clinical study[J]. Signal Transduct Target Ther, 2020,5(1):209.
[12]van Beijnum JR, Buurman WA, Griffioen AW. Convergence and amplification of toll-like receptor (TLR) and receptor for advanced glycation end products (RAGE) signaling pathways via high mobility group B1 (HMGB1). Angiogenesis. 2008;11(1):91-9.